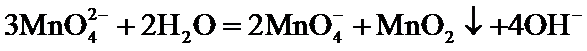2020山东新高考化学答案解析
1.实验室中下列做法错误的是
答案:D
2.下列叙述不涉及氧化还原反应的是
答案:B
3.短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高能级电子数的2倍,Z可与X形成淡黄色化合物Z2X2,Y、W最外层电子数相同。下列说法正确的是
答案:C
4.下列关于C、Si及其化合物结构与性质的论述错误的是
答案:C
5.利用下列装置(夹持装置略)进行实验,能达到实验目的的是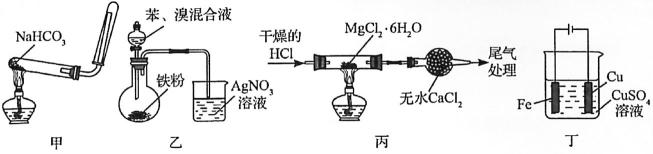
答案:C
6.从中草药中提取的 calebin A(结构简式如下)可用于治疗阿尔茨海默症。下列关于 calebin A的说法错误的是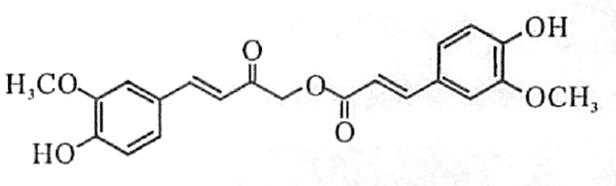
答案:D
7.B3N3H6(无机苯)的结构与苯类似,也有大π键。下列关于B3N3H6的说法错误的是
答案:A
8.实验室分离Fe3+和Al3+的流程如下: 已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6℃)中生成缔合物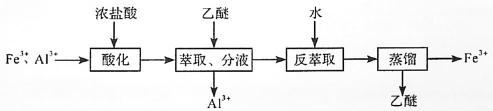
 。下列说法错误的是
。下列说法错误的是
答案:A
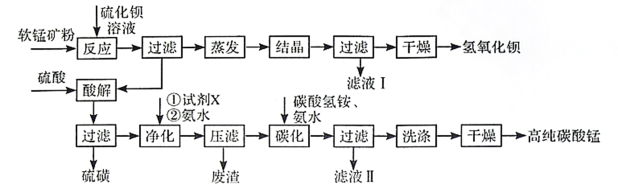
9.以菱镁矿(主要成分为MgCO3,含少量SiO2/Fe2O3和Al2O3)为原料制备高纯镁砂的工艺流程如下: 已知浸出时产生的废渣中有SO2、Fe(OH)3和Al(OH)3。下列说法错误的是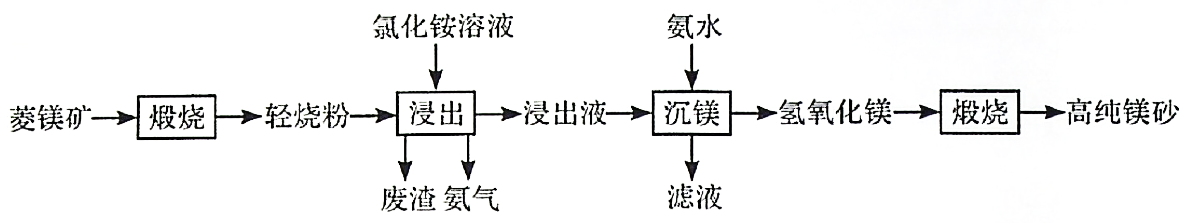
答案:B
11.下列操作不能达到实验目的的是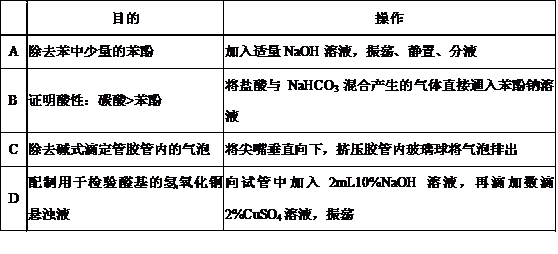
答案:BC
12.α-氰基丙烯酸异丁酯可用作医用胶,其结构简式如下。下列关于α-氰基丙烯酸异丁酯的说法错误的是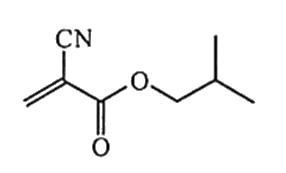
答案:C
13.采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是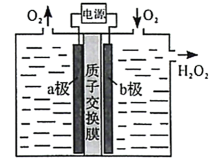
答案:D
15.25℃时,某混合溶液中 ,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和lgc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是
,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和lgc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是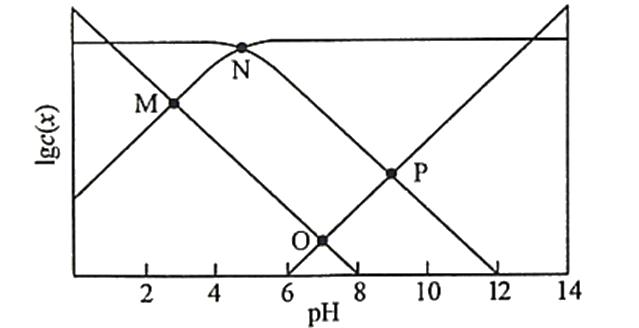
答案:BC
(1)增大接触面积,充分反应,提高反应速率;
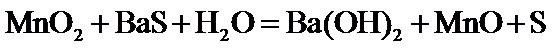
(2)过量的MnO2消耗了产生的Ba(OH)2
(3)蒸发
(4)H2O2;4.9
(5)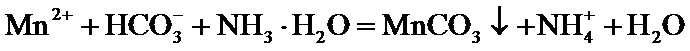
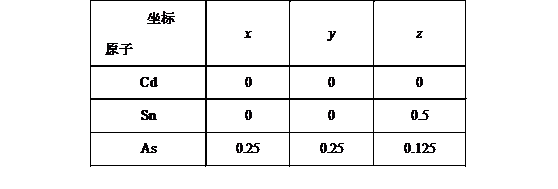
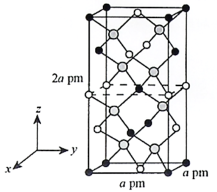
(1)正四面体形;分子晶体(2)NH3、AsH3、PH3;AsH3、PH3、NH3;NH3、PH3、AsH3(3)6;1(4)4;(0.5,0,0.25)、(0.5,0.5,0);4
(1)+40.9
(2)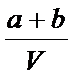 ;
;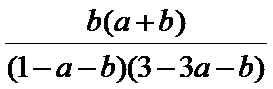
(3)乙;p1、p2、p3;T1时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有影响
(4)A
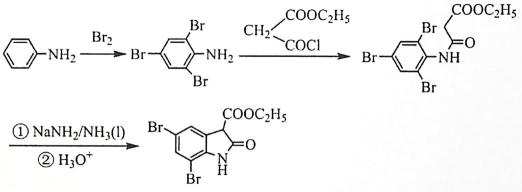
19.(12分)化合物F是合成吲哚-2-酮类药物的一种中间体,其合成路线如下: 知:Ⅰ. Ⅱ. Ⅲ. 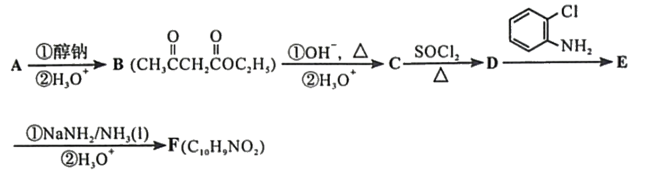
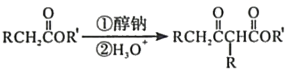
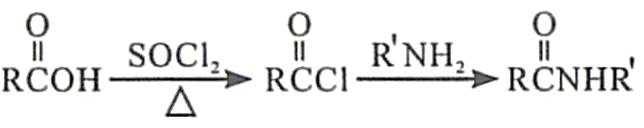
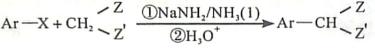
答案:
1)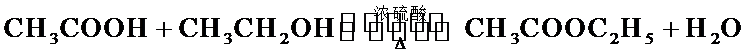
及时蒸出产物(或增大乙酸或乙醇的用量);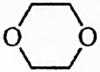
(2)取代反应;羰基、酰胺基
(3)CH3COCH2COOH;
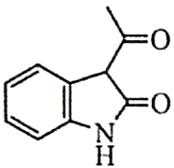
(4)
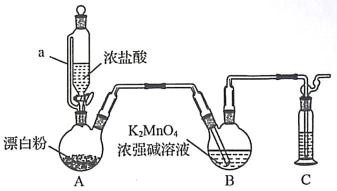
(1)平衡气压,使浓盐酸顺利滴下; NaOH溶液;
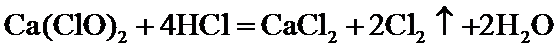
(2)在装置A、B之间加装盛有饱和食盐水的洗气瓶
(3)酸式;C
(4) ;B、D
;B、D



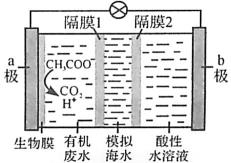
 );第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
);第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是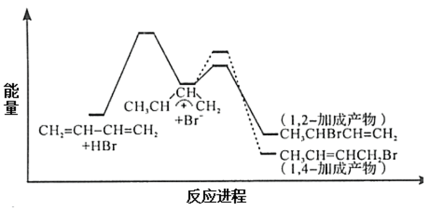

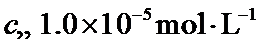 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
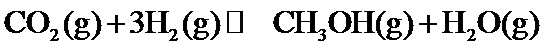
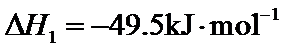
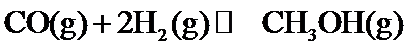
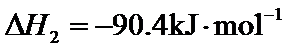
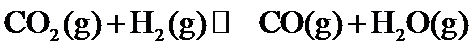
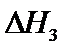
 。
。